Auk tækni hefur myndun glýkósíða alltaf vakið áhuga vísindanna, þar sem hún er mjög algeng efnahvörf í náttúrunni. Nýlegar greinar eftir Schmidt, Toshima og Tatsuta, sem og margar heimildir sem þar eru vitnað í, hafa fjallað um fjölbreytt úrval möguleika í myndun.
Við myndun glýkósíða eru fjölsykraþættir sameinaðir kjarnsækjum, svo sem alkóhólum, kolvetnum eða próteinum. Ef þörf er á sértækri viðbrögðum við einn af hýdroxýlhópunum í kolvetni verður að vernda allar aðrar aðgerðir í fyrsta skrefinu. Í meginatriðum geta ensím- eða örverufræðileg ferli, vegna sértækni þeirra, komið í stað flókinna efnafræðilegra verndar- og afverndunarskrefa til að sértækt fjarlægja glýkósíð á ákveðnum svæðum. Hins vegar, vegna langrar sögu alkýlglýkósíða, hefur notkun ensíma við myndun glýkósíða ekki verið mikið rannsökuð og beitt.
Vegna afkastagetu hentuga ensímkerfa og mikils framleiðslukostnaðar er ensímmyndun alkýlpólýglýkósíða ekki tilbúin til að uppfærast á iðnaðarstig og efnafræðilegar aðferðir eru æskilegri.
Árið 1870 greindi Macolley frá myndun „asetóklórhýdrósa“ (1, mynd 2) með efnahvarfi dextrósa (glúkósa) við asetýlklóríð, sem að lokum leiddi til sögunnar um myndun glýkósíða.
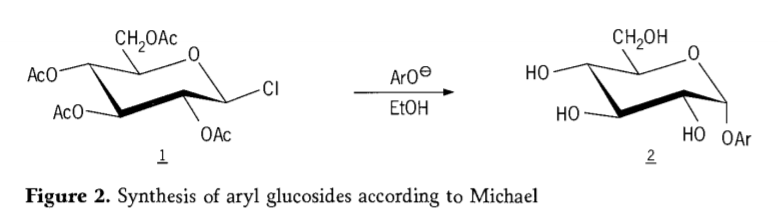
Tetra-0-asetýl-glúkópýranósýl halíð (asetóhalóglúkósar) reyndust síðar vera gagnleg milliefni fyrir staðbundna myndun hreinna alkýlglúkósíða. Árið 1879 tókst Arthur Michael að búa til ákveðin, kristöllunarhæf arýlglýkósíð úr milliefnum Colley og fenólötum. (Aro-, mynd 2).
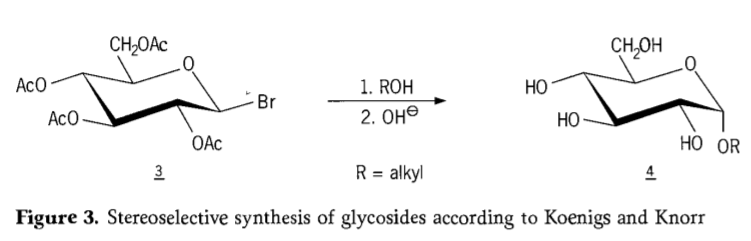
Árið 1901 kynntu W. Koenigs og E. Knorr til sögunnar endurbætt aðferð Michaels til að mynda fjölbreytt úrval kolvetna og hýdroxýlaglýkona, þegar W. Koenigs og E. Knorr kynntu til sögunnar endurbætt aðferð sína til að mynda sértæka glýkósíðmyndun (mynd 3). Viðbrögðin fela í sér SN2 skiptingu á anómera kolefnisatóminu og eiga sér stað með sértækri myndun, sem myndar til dæmis α-glúkósíð 4 úr β-anómera aseóbrómóglúkósa milliefnisins 3. Koenigs-Knorr myndunin fer fram í návist silfur- eða kvikasilfurshvata.
Árið 1893 lagði Emil Fischer til grundvallarauðbreytta aðferð við myndun alkýlglúkósíða. Þetta ferli er nú vel þekkt sem „Fischer glýkósíðering“ og felur í sér sýruhvataða efnahvörf glýkósa og alkóhóla. Sérhver söguleg frásögn ætti þó einnig að innihalda fyrstu tilkynntu tilraun A. Gautier árið 1874 til að umbreyta dextrósa með vatnsfríu etanóli í viðurvist saltsýru. Vegna villandi frumefnagreiningar taldi Gautier sig hafa fengið „díglúkósa“. Fischer sýndi síðar fram á að „díglúkósi“ Gautiers var í raun aðallega etýlglúkósíð (Mynd 4).
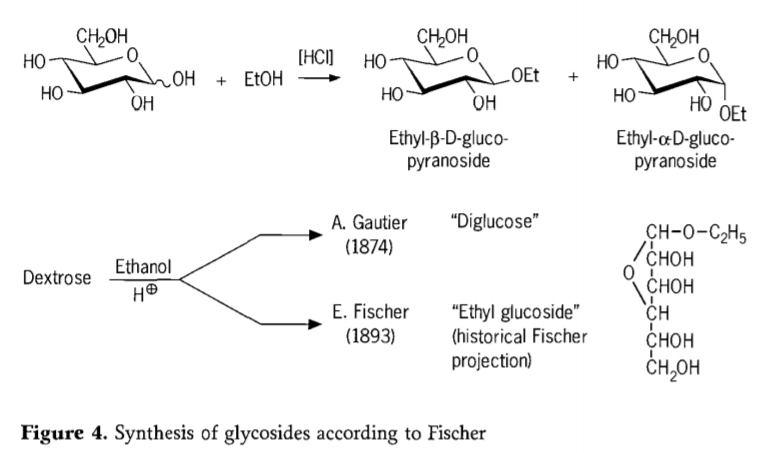
Fischer skilgreindi uppbyggingu etýlglúkósíðs rétt, eins og sjá má af sögulegu fúranósíðformúlunni sem lögð var til. Reyndar eru Fischer glýkósíðmyndunarafurðir flóknar, aðallega jafnvægisblöndur af α/β-anómerum og pýranósíð/fúranósíð ísómerum sem einnig innihalda handahófskenndar tengdar glýkósíðólígómerar.
Þar af leiðandi er ekki auðvelt að einangra einstakar sameindategundir úr Fischer-hvarfblöndum, sem hefur verið alvarlegt vandamál í fortíðinni. Eftir nokkrar umbætur á þessari myndunaraðferð tók Fischer síðar upp Koenigs-Knorr myndunina í rannsóknum sínum. Með þessari aðferð voru E. Fischer og B. Helferich fyrstir til að skýra frá myndun langkeðju alkýlglúkósíðs sem sýnir yfirborðsvirka eiginleika árið 1911.
Strax árið 1893 hafði Fischer réttilega tekið eftir mikilvægum eiginleikum alkýlglýkósíða, svo sem mikilli stöðugleika þeirra gagnvart oxun og vatnsrofi, sérstaklega í mjög basískum miðlum. Báðir eiginleikar eru verðmætir fyrir alkýlpólýglýkósíð í notkun sem yfirborðsvirk efni.
Rannsóknir tengdar glýkósíðmyndunarviðbrögðum eru enn í gangi og nokkrar áhugaverðar leiðir til glýkósíða hafa verið þróaðar að undanförnu. Sumar af aðferðunum við myndun glýkósíða eru teknar saman á mynd 5.
Almennt má skipta efnafræðilegum glýkósíðunarferlum í ferli sem leiða til flókins jafnvægis í oligómerum í sýruhvötuðum glýkósýlskiptum.
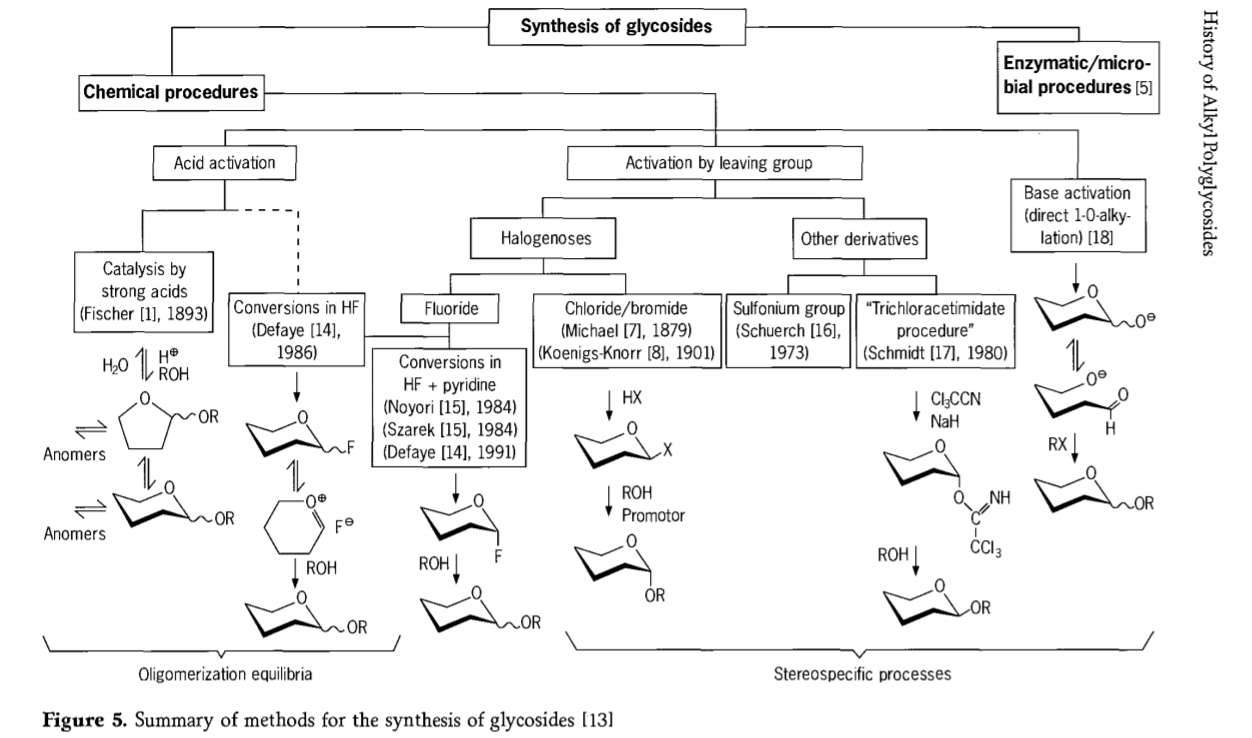
Viðbrögð á viðeigandi virkjuðum kolvetnisundirlögum (Fischer glýkósíðviðbrögð og vetnisflúoríð (HF) viðbrögð með óvarðum kolvetnissameindum) og hvarfhraðastýrð, óafturkræf og aðallega staðbundin skiptiviðbrögð. Önnur gerð aðferðar getur leitt til myndunar einstakra tegunda frekar en í flóknum blöndum af viðbrögðum, sérstaklega þegar þau eru notuð ásamt varðveisluhópatækni. Kolvetni geta skilið eftir hópa á utanlegs kolefni, svo sem halógenatóm, súlfónýl eða tríklórasetímídathópa, eða verið virkjuð af bösum áður en þau eru umbreytt í tríflatestra.
Í þeim tilfellum þar sem glýkósíðeringar eiga sér stað í vetnisflúoríði eða í blöndum af vetnisflúoríði og pýridíni (pýridíníum pólý [vetnisflúoríð]), myndast glýkósýlflúoríð in situ og umbreytast mjúklega í glýkósíð, til dæmis með alkóhólum. Vetnisflúoríð hefur reynst vera mjög virkjandi, ekki niðurbrotsefni; jafnvægisþétting (ólígómerun) sést svipað og í Fischer ferlinu, þó að hvarfferlið sé líklega öðruvísi.
Efnafræðilega hrein alkýlglýkósíð henta aðeins fyrir mjög sérstök verkefni. Til dæmis hafa alkýlglýkósíð verið notuð með góðum árangri í lífefnafræðilegum rannsóknum til kristöllunar himnupróteina, svo sem þrívíddarkristöllun poríns og bakteríóródópsíns í viðurvist oktýl β-D-glúkópýranósíðs (frekari tilraunir byggðar á þessu verki leiddu til Nóbelsverðlauna í efnafræði fyrir Deisenhofer, Huber og Michel árið 1988).
Við þróun alkýlpólýglýkósíða hafa staðbundin sértæk aðferð verið notuð á rannsóknarstofustigi til að mynda fjölbreytt fyrirmyndarefni og rannsaka eðlis- og efnafræðilega eiginleika þeirra. Vegna flækjustigs þeirra, óstöðugleika milliefna og magns og mikilvægs eðlis úrgangsefna, myndi myndun Koenigs-Knorr-gerðarinnar og annarra verndarhópatækni skapa veruleg tæknileg og efnahagsleg vandamál. Fischer-gerð ferli eru tiltölulega minna flókin og auðveldari í framkvæmd á viðskiptalegum skala og eru því ákjósanleg aðferð til framleiðslu á alkýlpólýglýkósíðum í stórum stíl.
Birtingartími: 12. september 2020





